6,15 € (Sin IVA)
Essai rapide des antigènes diagnostiques COVID-19 (antigènes SARS-CoV-2)
C'est un test antigène pour la détection du virus actif.
La détection du virus est effectuée dans les 7 premiers jours de contagion.
Essayez le nasopharyngéal.
Les résultats de l ' essai en 15 minutes
Chaque pack comprend 1 test + 1 hysope nasal + 1 tube + 1 bouteille réactive
2,94 € (Sin IVA)
Test antigène rapide pour le diagnostic COVID-19 (SARS-CoV-2).
Le boîtier de test rapide Coronavirus Ag (Swab) est un test immunochromatographique in vitro pour la détection qualitative de l'antigène nucléocapsidique de protéine SARS-CoV-2 dans les échantillons d'hisopos nasopharyngéal (NP) directement ou après l'hisopos ont été ajoutés aux moyens de transport viral des personnes soupçonnées de COVID-19 par leur fournisseur de santé.
Son objectif est d'aider à diagnostiquer les infections SARSCoV-2 rapidement. Le boîtier de test rapide Coronavirus Ag (Swab) ne différencie pas entre SARS-CoV et SARS-CoV-2.
RÉSUMÉ ET EXPLICATION
Le nouveau coronavirus appartient au genre β. COVID-19 est une maladie infectieuse respiratoire aiguë. Les gens sont généralement vulnérables.
Actuellement, les patients infectés par le nouveau coronavirus sont la principale source d'infection; les personnes infectées par l'asymptomatique peuvent également être une source infectieuse.
Selon la recherche épidémiologique actuelle, la période d'incubation est de 1 à 14 jours, principalement de 3 à 7 jours. Les principales manifestations sont la fièvre, la fatigue et la toux sèche. Dans certains cas, il y a la congestion nasale, la sécrétion nasale, la gorge aiguë, la myalgie et la diarrhée.
Ce test vise la détection de l'antigène protéique du nucléocápside SARSCoV-2. L'antigène est généralement détectable dans les échantillons des voies respiratoires supérieures pendant la phase aiguë de l'infection.
Le diagnostic rapide de l'infection SARS-CoV-2 aidera les professionnels de la santé à traiter les patients et à contrôler la maladie de manière plus efficace et efficiente.
PRINCIPE DES TRAVAUX
Coronavirus Ag (Swab) est un test de membrane immunochromatographique qui utilise des anticorps monoclonaux très sensibles pour détecter la protéine nucléocápside SARS-CoV-2 dans un hysop nasopharyngéal (NP).
La bande réactive se compose des parties suivantes : tampon d'échantillonnage, plaque réactive, membrane de réaction et plaque d'absorption.
Le coussin réactif contient l'or colloïdal combiné avec des anticorps monoclonaux contre la protéine du nucléocápside du SARS-CoV-2; la membrane de réaction contient les anticorps secondaires pour la protéine nucléocápside du SARS-CoV-2.
La bande entière est fixée dans un dispositif en plastique TECHNIQUE Ed.1/2020 2.
Lorsque l'échantillon est ajouté à la boîte d'échantillonnage, les conjugués séchés dans la plaque réactive se dissoudent et migrent avec l'échantillon.
Si l'antigène SARS-CoV-2 se produit dans l'échantillon, un complexe formé entre le conjugué anti-SARS-2 et le virus sera capturé par les anticorps monoclonaux anti-SARS-2 spécifiques enduits dans la région de la ligne d'essai (T). L'absence de la ligne T suggère un résultat négatif.
Pour servir de contrôle de procédure, une ligne rouge apparaîtra toujours dans la région de la ligne de commande (C) qui indique que le volume approprié de l'échantillon a été ajouté et que l'absorption de la membrane a eu lieu.
SUMINISTRAIRE
- 1 cassette
- 1 hysop stérile
- 1 tube d ' extraction et tuyau d ' essai
- 1 poste de travail
- 1 tampons
- 1 paquet
MATERIAL REQUERED BUT NOT SUMINISTRED
- Attention, minuterie ou minuterie
WARNINGS AND PRECAUTIONS:
- Juste pour un diagnostic in vitro.
- Le dispositif d ' essai doit rester dans le sac scellé jusqu ' à son utilisation.
- N'utilisez pas le kit après votre date d'expiration.
- Hisopos, tubes et dispositifs d'essai sont d'une seule utilisation.
- Le tampon d'extraction contient une solution avec un conservateur (zéro sodium à 0,09%). Si la solution entre en contact avec la peau ou les yeux, rincer avec de grandes quantités d'eau.
- Les solutions d'azure de sodium peuvent réagir explosivement avec des tuyaux en plomb ou en cuivre. Utilisez de grandes quantités d'eau pour jeter des solutions éliminées par un évier.
- Ne pas échanger ou mélanger des composants de différents lots de kit.
- Lors de la collecte d'un échantillon de torunda nasopharyngea, utilisez la torunda nasopharyngea fournie dans le kit.
- Pour obtenir des résultats exacts, n'utilisez pas d'échantillons sanguins ou trop visqueux.
- Utilisez des vêtements de protection appropriés, des gants et une protection oculaire/face lorsque vous manipulez le contenu de ce kit.
- L'humidité et la température peuvent affecter négativement les résultats.
- Les matériaux d ' essai utilisés doivent être éliminés conformément à la réglementation locale.
ET STABILITÉ
- Le kit peut être stocké à température ambiante ou refroidi (2-30 °C).
- Ne pas geler l'un des composants du kit d'essai.
- N'utilisez pas le dispositif d'essai et les réactifs après la date d'expiration.
- Revenir immédiatement après avoir enlevé un dispositif d ' essai.
- Les dispositifs d ' essai qui sont sortis du réservoir sec pendant plus d ' une heure doivent être supprimés.
SPECIME RECOLECTION
Utilisez l'hysope nasopharyngé fourni dans le kit.
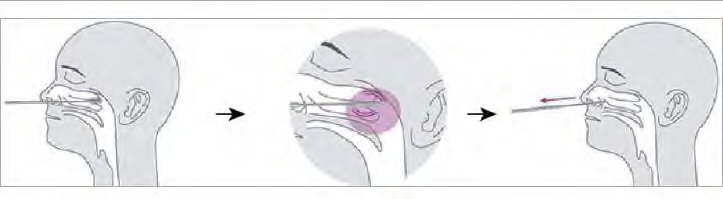
- Insérer soigneusement l'hysope dans la narine du patient, atteignant la surface du nasopharynx postérieur qui présente la plus grande sécrétion sous inspection visuelle.
- Frottez à la surface du nasopharynx postérieur. Tournez l'hysope plusieurs fois.
- Retirer l'hisopo de la cavité nasale.
PROCÉDURES DE PRÉPARATION DES FEMMES
- Insérer le tube d'extraction d'essai dans la station de travail dans ce produit. Assurez-vous que le tube est ferme et atteint le bas de la station de travail.
- Ajouter 0,3 mL (environ 10 gouttes) du tampon d'extraction de l'échantillon dans le tube d'extraction.
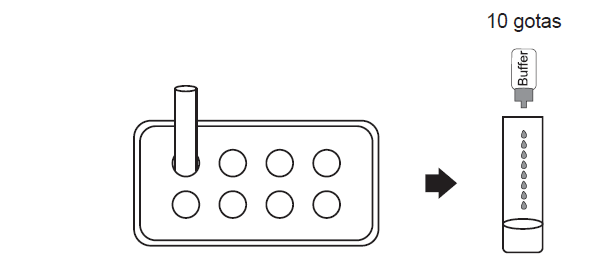
- Insérer l'hysope dans le tube d'extraction contenant 0,3 mL du tampon d'extraction.
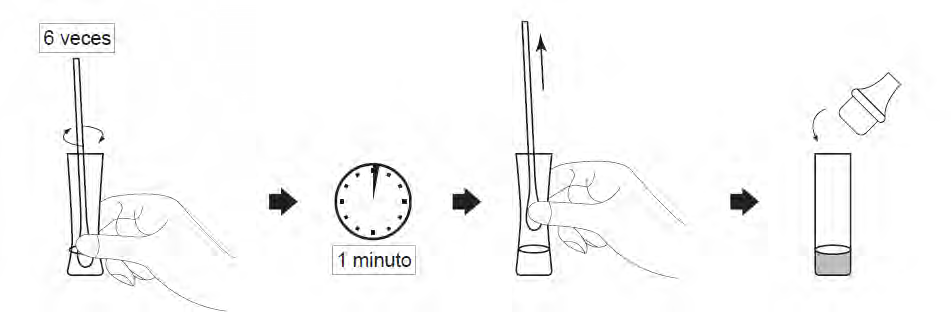
- Roulez l'hysope au moins 6 fois en appuyant sur la tête contre le fond et le côté du tube d'extraction.
- Laisser la toronde dans le tube d'extraction pendant 1 minute.
- Pressez le tube plusieurs fois avec vos doigts de l'extérieur du tube pour plonger l'hysop. Retirer la toronde. La solution extraite sera utilisée comme échantillon d ' essai.
TRANSPORT ET ALMACENAMIENT
Les échantillons doivent être analysés dès que possible après la collecte. Si le transport des échantillons avec le transport viral (VTM) est nécessaire, une dilution minimale de l ' échantillon est recommandée, car la dilution peut entraîner une diminution de la sensibilité de l ' essai. Dans la mesure du possible, la meilleure chose est de 1 millilitre ou moins pour éviter une dilution excessive de l'échantillon du patient. En tenant l'hysope, retirez le bouchon du tube.
Insérer l'hysope dans le tube jusqu'à ce que le point de rupture soit rangé avec l'ouverture du tube. Plier l'axe de l'hysope à un angle de 180 degrés pour le casser au point de rupture. Il est possible que l'axe de l'hysope soit légèrement tourné pour terminer la rupture. Selon les données générées avec le virus de la grippe, l'hisopos nasopharyngé en VTM est stable jusqu'à 72 heures à une température de 2 ° à 8 °C.
Remarque: En utilisant le moyen de transport viral (VTM), il est important de s'assurer que la VTM contenant l'échantillon est chaude à température ambiante. Les échantillons de froid ne circulent pas correctement et peuvent entraîner des résultats erronés ou invalides. Il faudra plusieurs minutes pour apporter un échantillon froid à la température ambiante.
PROCÉDURES DE TRAVAIL
Autorise le dispositif d ' essai, l ' échantillon d ' essai et le tampon à équilibrer à température ambiante (15-30 °C) avant l ' essai.
- Retirer le dispositif d'essai de sac scellé juste avant l'essai et le placer dans le banc de travail.
- Insérer fermement une buse de filtre dans le tube d'extraction de l'échantillon.
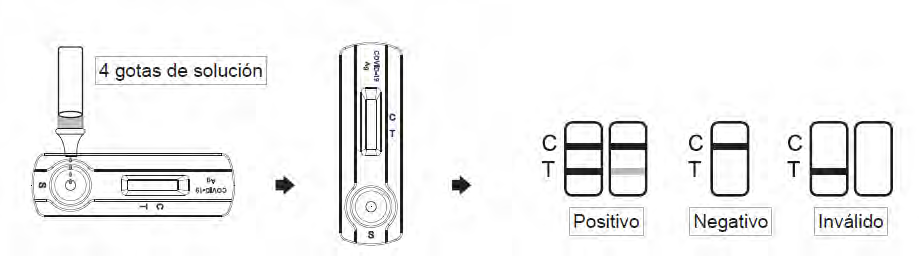
- Investir le tube d'extraction de l'échantillon et ajouter 4 gouttes (environ 100 μL) de l'échantillon d'essai en resserrant le tube de solution extrait dans la fenêtre de l'échantillon.
- Attendez que les groupes de couleurs se présentent. Le résultat doit être lu en 15 minutes. Ne pas interpréter le résultat après 20 minutes.
INTERPRETATION OF RESULTS
POSITIVE:
La présence de deux lignes comme ligne de commande (C) et ligne de test (T) dans la fenêtre de résultats indique un résultat positif.
NEGATIVE:
La présence d'une seule ligne de commande (C) dans la fenêtre de résultats indique un résultat négatif.
INVOLIDE:
Si la ligne de commande (C) n'est pas visible dans la fenêtre de résultats après l'essai, le résultat est considéré comme nul. Certaines causes de résultats invalides sont dues à l ' incapacité de suivre les instructions correctement ou l ' essai peut s ' être détérioré au-delà de la date d ' expiration. Il est recommandé que l'échantillon soit analysé à nouveau à l'aide d'un nouveau test.
NOTES:
- L'intensité de la couleur dans la région de la ligne d'essai (T) peut varier en fonction de la concentration d'analyse présente dans l'échantillon. Par conséquent, tout ton de couleur dans la région de la ligne de test (T) devrait être considéré comme positif. Notez que c'est un test qualitatif seulement, et vous ne pouvez pas déterminer la concentration des analites dans l'échantillon.
- Le volume insuffisant de l'échantillon, la procédure de fonctionnement incorrecte ou les essais périmés sont les raisons les plus probables de la défaillance de la bande témoin.
CONTRÔLE DE QUALITÉ
Un contrôle de procédure est inclus dans l ' essai. Une ligne rouge qui apparaît dans la région de la ligne de commande (C) est le contrôle interne de la procédure. Confirmer le volume d'échantillon suffisant et la technique de procédure correcte. Les normes de contrôle ne sont pas fournies avec cet essai. Toutefois, il est recommandé que des contrôles positifs et négatifs viennent d ' une autorité compétente locale et soient testés comme une bonne pratique de laboratoire, confirment la procédure d ' essai et vérifient l ' efficacité de l ' essai.
LIMITATIONS DE PROCÉDURE
- L'étiologie de l'infection respiratoire causée par des microorganismes autres que SARS-CoV-2 ne sera pas établie avec ce test. Coronavirus Ag Quick Test Case (Torunda) est en mesure de détecter SARS-CoV-2 à la fois viable et non viable. La performance du coronavirus Ag Quick Test Case (Torunda) dépend de la charge antigène et peut ne pas être corrélée avec les résultats de la récolte virale effectuée dans le même échantillon.
- Le non-respect de la procédure d ' essai peut nuire à l ' efficacité de l ' essai et/ou invalider le résultat de l ' essai.
- Si le résultat du test est négatif et que les symptômes cliniques persistent, des tests supplémentaires sont recommandés avec d'autres méthodes cliniques. Un résultat négatif n ' exclut pas à tout moment la présence d ' antigènes SARS-CoV-2 dans l ' échantillon, car ils peuvent être présents en dessous du niveau minimal de détection des essais ou si l ' échantillon a été recueilli ou transporté incorrectement.
- Comme pour tous les tests diagnostiques, un médecin doit faire un diagnostic confirmé après que toutes les conclusions cliniques et de laboratoire ont été évaluées.
- Les résultats positifs ne règlent pas les coinfections avec d'autres agents pathogènes.
- Les résultats positifs ne différencient pas entre SARS-CoV et SARS-CoV-2.
- Les résultats négatifs devraient être considérés comme présumés et confirmés par un essai moléculaire autorisé par la FDA, si nécessaire, pour la gestion clinique, y compris le contrôle des infections.
CLAIMS
1. Sensibilité clinique, spécificité et précision
Le coronavirus Ag Quick Test Case (Torunda) a été évalué avec des échantillons obtenus de patients. Un essai moléculaire a été utilisé comme méthode de référence. Les résultats montrent que le coronavirus Ag Quick Test Case (Torunda) a une grande précision relative globale.
Tableau 1: Coronavirus Ag Test rapide vs PCR
| Méthode | PCR | Total des résultats | ||
| Coronavirus Ag Essai rapide Cassette |
Résultats | Positif | Négatif | |
| Positif | 39 | 0 | 39 | |
| Négatif | 6 | 116 | 122 | |
| Total des résultats | 45 | 116 | 161 | |
Sensibilité relative : 86,7 %
Spécification relative: 100%
Précision: 96,3%
SIMBOLOGIE
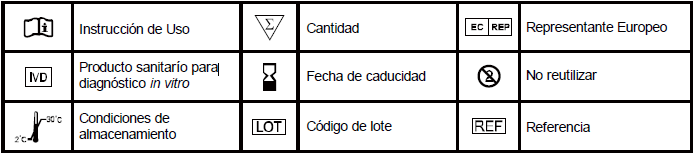
ON SEKURECO
Sekureco est une entreprise née en 2016 grâce à la passion de plusieurs techniciens spécialisés dans la prévention et la sécurité au travail et face au manque d'entreprises vraiment spécialisées dans la protection du travail sur le marché.

















@CUSTOMER_NAME@
@AUTHOR_PROFILE@ @COMMENT_ISO_COUNTRY@ @VERIFY_PURCHASE@@COMMENT_TITLE@
@COMMENT_COMMENT@